Immunité aux fréquences RFID pour les Dispositifs Médicaux avec LCIE
En 2018, la FDA (Food and Drug Administration) pointe le manque d’immunité de certains dispositifs médicaux aux systèmes RFID.
Afin de compléter les essais IEC 60601-1-2 Ed4.1, la FDA impose l’application de la norme américaine AIM 7351731.
L’IEC 60601-1-2 fixe des exigences d’immunité dans la gamme de fréquence de 150kHz à 6GHz, la norme AIM 7351731 décrit des tests complémentaires d’immunité avec la particularité d’utiliser les signaux RFID au lieu de modulation générique.
Voici les niveaux, fréquences et signaux RFID utilisés :

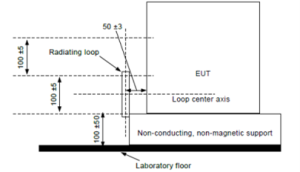
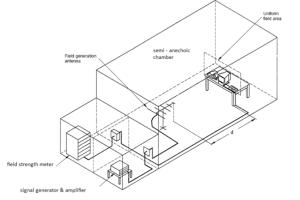
Les essais calquent des méthodes connues et accréditées COFRAC, IEC 61000-4-39 et IEC 61000-4-3 :
A la suite de l’accréditation pour l’IEC 61000-4-39, les équipes du LCIE Bureau Veritas de Moirans (38) ont acquis un logiciel pilotant leurs générateurs de signaux afin de créer les signaux RFID conformes aux standards du domaine.
A ce jour, les essais sont réalisables dans le laboratoire de Moirans, le chiffrage est à considérer avec un nombre de « fenêtre » et de face comme la 4-39 ; pour simplifier un chiffrage pour un produit « classique » de 40cm x 40cm x40cm prend en compte 1.5jrs Essai + Rapport
Pour les produits médicaux avec de la Radio, la FDA rajoute une norme d’analyse ANSI C63.27 pour démontrer la capacité de l’appareil radio à coexister avec son environnement et les autres appareils RF autour de lui.
Cela se « résume » à une analyse de la RF, des attentes en termes de qualité/réception et des radios pouvant être utilisées autour ; ensuite un essai de blocking est réalisé avec des signaux RF réel.
Fabricant de produits médicaux, vous exportez aux Etats-Unis ? Vous devriez être touché, contactez Stéphane RANCHON, stephane.ranchon@bureauveritas.com ou, Nathalie OLAGNON-RICHARD, nathalie.olagnon-richard@bureauveritas.com pour en savoir plus !